IPTG誘導(dǎo)原理(原核表達)
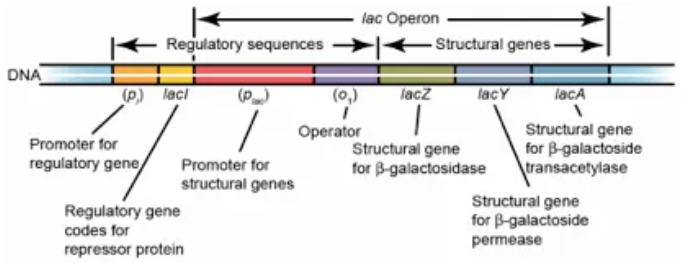
乳糖操縱子結(jié)構(gòu)基因
IPTG誘導(dǎo)原理.
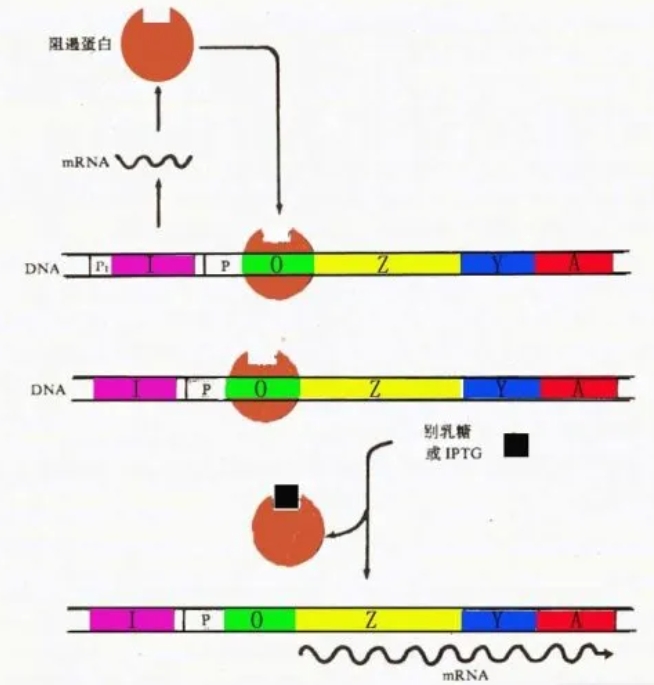
Lac阻遏物是一種具有4個相同亞基的四級結(jié)構(gòu)蛋白,都有一個與誘導(dǎo)劑結(jié)合的位點。在沒有乳糖存在時,lac操縱子(元)處于阻遏狀態(tài),Lac阻遏物(即下圖中的阻遏蛋白)能與操縱基因O結(jié)合,阻礙RNA聚合酶與P序列結(jié)合,阻止了轉(zhuǎn)錄的路徑,從而抑制轉(zhuǎn)錄啟動。而當有誘導(dǎo)劑(這里指IPTG)存在時,誘導(dǎo)劑可與阻遏蛋白結(jié)合,使阻遏蛋白構(gòu)象發(fā)生變化,導(dǎo)致阻遏物從操縱基因O上解離下來,RNA聚合酶不再受阻礙,啟動子P開始發(fā)生轉(zhuǎn)錄,啟動反應(yīng)開始發(fā)生轉(zhuǎn)錄。
 、
、IPTG誘導(dǎo)表達實驗方法
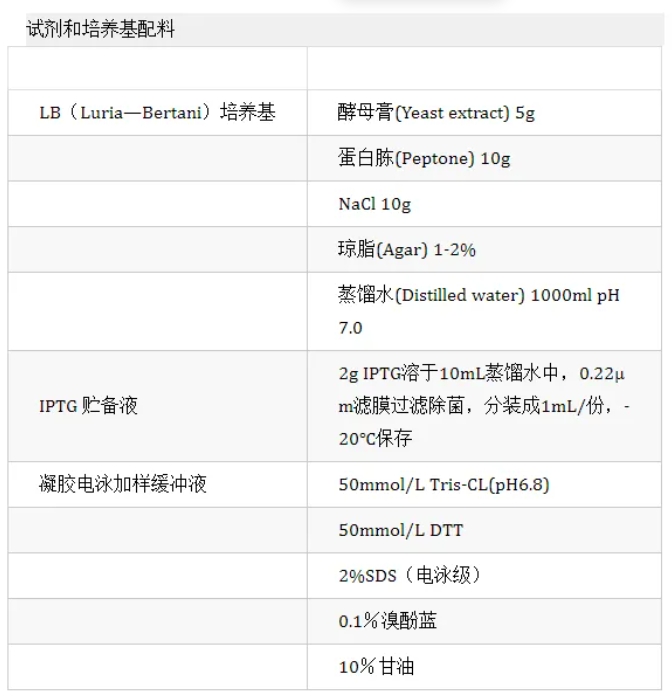
原核表達鑒定詳細實驗步驟
拿到質(zhì)粒,離心(3000r/min;2min) 在質(zhì)粒中加入TE【使質(zhì)粒最終加入到110μL感受態(tài)細胞中的量為80-100ng,據(jù)此確定加入TE的量】,一般為(1μg質(zhì)粒加20μLTE;2μg質(zhì)粒加50μLTE;5μg質(zhì)粒加100μL TE) 將質(zhì)粒與TE混勻,吸取2μL混液與感受態(tài)細胞混勻 將感受態(tài)細胞放入冰箱(4℃)中,30min 取出后立即放入水浴鍋中(42℃),熱激90s, 再次放入冰箱(4℃)中,3min 拿出后取200μL的LB液體培養(yǎng)基加入到已轉(zhuǎn)入質(zhì)粒的感受態(tài)細胞中 放入搖床(37℃; 195r) 中, 30nim至60min; (最佳45min) 取出離心(3000r/min;2min) 去掉200μL的上清,留100μL左右上清懸浮沉淀,吸取50μL懸液涂平板,【先將對應(yīng)抗性的平板放入培養(yǎng)箱(37℃)中預(yù)熱20min】 把平板放入培養(yǎng)箱(37℃),過夜(12h至16h)
每個平板挑取單菌落至4支對應(yīng)抗性的LB(4ml)試管中,編號為“0”“1”“2”“3” 將試管放入搖床(37℃;195r) 中,【單抗3h左右;雙抗4h左右;剛開始用可見分光光度計測OD值;熟練后可目測(背光下,以試管中的槍頭為例,剛剛看不見槍頭即可)】,測OD值(0.6至0.8) 從“0”號管中取700μL懸液加入到100μL(C=80%)的保種甘油中,震勻,放入冰箱(-20℃)凍存 在每組菌的“1”“2”“3”號試管中分別加入2μL的IPTG【終濃度0.5mM最適,可根據(jù)日后表達摸索】 視不同的載體選擇適合的表達環(huán)境【PET/PGEX:15℃表達過夜;25℃表達6h;37℃表達3h至4h(4支試管,“0”“1”號試管15℃表達過夜;“2”“3”試管37℃表達3h至4h)。Pcold:【全部15℃表達過夜】
3.表達鑒定第三天,全菌的表達鑒定分析,注意控制溶質(zhì)的量及溶液黏度
從每組4支的試管中均取500μL菌液加入到1.5ml離心管中,【若OD值不一樣,值小的可多取】離心(6000r/min),5min, 去上清,留沉淀【沉淀少的,可再取菌液離心,盡量使沉淀量接近】 在每個離心管中加入500μL的DDH2O,懸浮沉淀,離心(6000r/min),5min, 去上清,留沉淀 在每支離心管中加入45μL的1×PBS和45μL的2×Loading Buffer懸浮沉淀【當溶質(zhì)適量且均一的情況下,加入量不變;當溶質(zhì)多且粘稠時,應(yīng)使加入量增大,為降低粘度也可減少上液量】 放入煮樣器(100℃) 25min 取出后離心(6000r/min) 3min, 電泳檢測。 蛋白表達量不錯,進行蛋白純化.蛋白表達量低或者沒表達就菌株與質(zhì)粒、誘導(dǎo)條件、目的蛋白特性、培養(yǎng)環(huán)境及檢測環(huán)節(jié)五大類來進行排查分析。
科普文章均整理自網(wǎng)絡(luò),僅作知識分享,無商業(yè)用途。若有侵權(quán),請聯(lián)系后臺,提供文章標題、鏈接等信息,我們核實后會立即刪除,感謝理解。